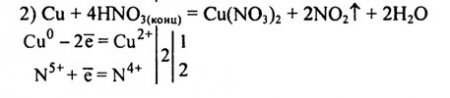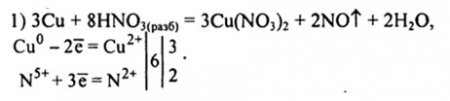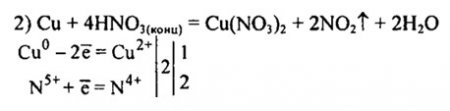Вариант 1
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
С →С02 →СаС03 →СаС12 →СаС03.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
С→СО2→ СаСО3→ CaCl2 → СаСО3
C+O2 → CO2
C0 -4e= C+4 восстановитель
O2 + 4e= 2O-2 окислитель
CO2+ CaO→CaCO3
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
N2 + ЗН2 2NH3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3H2 + N2 2NH3 + Q
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
Исходные вещества: 1 моль азота (молекула из 2 атомов азота), 3 моль водорода (молекула из 2 атомов водорода). Продукт реакции – аммиак, 2 моль. Молекула из 1 атома азота и 2 атомов водорода. Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Каталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) → CU(N03)2 + NO + Н20.
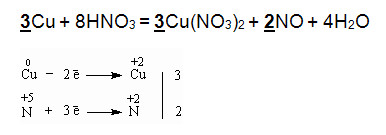
ЗАДАНИЕ 4
К раствору, содержащему 16 г сульфата меди (II), прибавили избыток железных опилок. Какая масса меди выделилась при этом?
CuSO4 + Fe = FeSO4 + Cu
n (CuSO4) = 16/160 = 0,1моль
n (CuSO4) = n (Cu) =0,1моль
m(Cu) = 0,1*64= 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
N2 → NO → N02 →HN03 →CU(N03)2.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
N2 + O2 = 2NO
N20 -4e= 2N+2 восстановитель
O20 +4e= 2O-2 окислитель
2NO + O2 = 2NO2
4NO2 + O2 + 2H2O = 4HNO3
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
3Cu0 + 8H++8NO3- = 3Cu2+ +6NO3- + 2NO + 4H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2N0 + 02 2N02 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNO3(КОНЦ) → Cu(N03)2 + N02 + Н20.
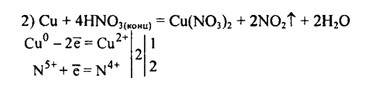
ЗАДАНИЕ 4
6,5 г цинка обработали достаточным количеством разбавленного раствора серной кислоты. Определите объем выделившегося водорода.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 6,5/65 = 0,1 моль
n(H2) = n(Zn) = 0,1 моль
V(H2) = 0,1*22,4 = 2,24 л
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
S → S02 →S03 H2S04 →BaS04.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
S+O2→ SO2
S0 -4e = S+4
O02 + 4e = 2O-2
2SO2+O2→2SO3
SO3+H2O→H2SO4
H2SO4+ BaCl2 = BaSO4↓ + 2HCl
SO42-+ Ba2+ = BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО – Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHц) → ZnS04 + H2S↑ + H20.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Определите количество вещества сульфата калия, полученного при сливании избытка раствора гидроксида натрия с раствором, содержащим 2 моль серной кислоты.
2KOH + H2SO4 = K2SO4 + H2O
n(H2SO4) = n(K2SO4) = 2 моль
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
Si → Si02 →Na2Si03 →H2Si03 →Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
1) Si + O2 = SiO2
Si0 -4е = Si+4 восстановитель
O20 +4е = 2O2- окислитель
2) SiO2 + Na2O = Na2SiO3
3) Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2H+ +SiO3 2- = H2SiO3 ↓
4) H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Н20(пар) + СО Н2 + С02 – Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→ N2 + Сu + Н20.
2NH3 + 3CuO -> 3Cu + N2 + 3H2O
N-3 -6е = N20 восстановитель
Cu+2 +2е =Cu0 окислитель
ЗАДАНИЕ 4
10 г оксида магния обработали раствором азотной кислоты. Какая масса соли образовалась?
MgO + 2HNO3 = Mg(NO3)2 + H2O
n (MgO) = 10/40 =0,25 моль
n (MgO) = n (Mg(NO3)2) = 0,25 моль
m(Mg(NO3)2) = 0,25*148= 37 г
Вариант 1
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С → СН4 →С02 →СаС03 →… →СаС03.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
С + 2Н2 = СН4
СН4 + 2О2 = СО2 + 2Н2О
С-4 – 8е=С+4 восстановитель
О2 о +4е = 2О-2 окислитель
СО2 + СаО = СаСО3
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Ca2+ + 2HCO3- = CaCO3↓ + CO2 + H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2Fe + ЗС12 = 2FeCl3 + Q,
по всем изученным признакам классификации.
Определите окислитель и восстановитель, процессы окисления и восстановления.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →Cu(NO3)2 + … + Н20.
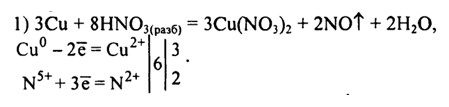
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили железные опилки. Какая масса меди выделилась?
CuSO4 + Fe = FeSO4 + Cu
m (CuSO4) = 160*0,1= 16 г
n(CuSO4) = 16/160 = 0,1 моль
m (Cu) =0,1 * 64 = 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 → Li3N →NO →N02 … →…→ Cu(NO3)2.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
1)N2+6Li->t,кат. ->2Li3N
2) 4Li3N + 5O2->t->4NO+6Li2O
N-3 -5e =N+2 восстановитель
O20 +4е= 2O-2 окислитель
3)2NO+O2->2NO2
4)4NO2+2H2O+O2->4HNO3
5) Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2А1 + 3S = A12S3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2Al + 3S = Al2S3 + Q
Al – 3e– = Al +III восстановитель
S+ 2e– = S –Il окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 3 моль серы тв.
Продукт: 1 моль сульфида алюминия (из 2 атомов алюминия, 3 атомов серы) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(KOHЦ) → Cu(N03)2 + … + Н20.
ЗАДАНИЕ 4
Достаточное количество цинка обработали 120 кг 10%-го раствора серной кислоты. Определите объем выделившегося газа.
Zn + H2SO4 = ZnSO4 + H2
m (H2SO4) = 120*0,1= 12кг= 12000 г
n(H2SO4) = 12000/98 = 122 моль
n(H2) = n(H2SO4) = 122 моль
V(H2) = 122*22,4 = 2742 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →S03 →…→ BaS04.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
Fe + S = FeS
2FeS + 3O2 = 2FeO + 2SO2
S-2 -6e = S+4 восстановитель
O20 +4е= 2O-2 окислитель
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + SO42- → BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
ЗСа + 2Р = Са3Р2 – Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3Са + 2Р = Са3Р2 – Q
Са – 2e– = Са +II восстановитель
Р + 3e– = Р –IlI окислитель
Эндотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль фосфора – тв., 3 моль кальция тв.
Продукт: 1 моль фосфида кальция (из 2 атомов фосфора, 3 атомов кальция) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOH4) → ZnS04 + … + Н20.
2H2SO4 + Zn = SO2↑ +ZnSO4 + 2H2O
Zn – 2e– = Zn +II восстановитель
S+6 + 2e– = S +4 окислитель
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии достаточного количества цинка с 200 г 10% -го раствора серной кислоты?
H2SO4 + Zn = Zn SO4 + H2 ↑
m (H2SO4) = 200*0,1= 20 г
n(H2SO4) = 20/98 = 0,2 моль
n(H2) = n(H2SO4) = 0,2 моль
V(H2) = 0,2*22,4 = 4,57л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si → Si02 →Na2Si03 →…→ Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
Si + O2 = SiO2
Si0 -4е = Si+4
O20 +4е= 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
Na2SiO3 + 2HCl = H2SiO3 + 2NaCl
2Н+ +SiO3 2- = H2SiO3 ↓
H2SiO3 = SiO2+ H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Fe203 + 2А1 = 2Fe + А1203 + Q,
по всем известным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Fe2O3 + 2Al = 2Fe + Al2O3 + Q
Al0 – 3e– = Al +III восстановитель
Fe+3 + 3e– = Fe 0 окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 1 моль оксида железа 3 (2 атома железа и 3 атома кислорода в ФЕ) тв.
Продукты: 2 моль железа, 1 моль оксида алюминия (из 2 атомов алюминия, 3 атомов кислорода в ФЕ) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + Сu + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
Достаточное количество оксида магния обработали 40 кг 10%-го раствора азотной кислоты. Какая масса соли образовалась?
2HNO3 + MgO = Mg(NO3)2 + H2O
m (HNO3) = 40000*0,1= 4000 г
n(HNO3) = 4000/63 = 63,5 моль
n(Mg(NO3)2) = n(HNO3)/2 = 31,7 моль
m (Mg(NO3)2) = 31,7*148 = 4698 г = 4,698 кг
Вариант 1
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С →СН4 → … →CaCO3→ … → CaCO3.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
С + 2Н2 = СН4
С0 +4е = С-4 окислитель
Н20 -2е = 2Н+1 восстановитель
СН4 + О2 = СО2 + Н2О
С-4 -8е = С+4 восстановитель
О20 +4е = 2О-2 окислитель
СО2 + СаО = СаСОз
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCO3+2H+→ Ca2+ +H2O + CO2↑
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Zn + 2НС1 = ZnCl2 + H2↑ + Q,
по всем изученным признакам классификации.
Рассмотрите реакцию с точки зрения ТЭД.
Zn+2HCl=ZnCl2+H2 + Q
Исходные вещества: 1 моль цинк, 2 моль соляной кислоты (1 атом водорода, 1 атом хлора в молекуле). Продукты реакции: 1 моль хлорида цинка (1 атом цинка, 2 атома хлора в ФЕ), 1 моль водорода (2 атома водорода).
Экзотермическая реакция
Цинк – тв., соляная кислота – ж., хлорид цинка тв. (раствор), водород – г.
Без катализатора
С изменением степеней окисления
Необратимая
2H++2Cl-+Zn0=Zn2++2Cl-+H20
2H++Zn0=Zn2++H20
ЗАДАНИЕ 3
Закончите уравнение ОВР, расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →.
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили избыток железных опилок. Какая масса меди выделилась, если выход продукта составил 90% от теоретически возможного?
Fe + CuSO4 = FeSO4 + Cu
m (CuSO4) = 160000*0,1= 16000 г
n (CuSO4) = 16000/160= 100 моль
n (CuSO4)= n (Cu) по уравнению (теор.) = 100 моль
n (Cu) = 100/0,9 = 90 моль (пр.)
m (Cu) = 90*64= 5760 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 →… →NO →N02 →… →Cu(N03)2.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
1)N2+3H2->t,кат. ->2NH3
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
2)4NH3+5O2->t,кат. ->4NO+6H2O
N-3 – 5е→N+2 восстановитель
O20 +4e→2O-2 окислитель
3)2NO+O2->2NO2
N+2 – 2е→N+4 восстановитель
O20 +4e→2O-2 окислитель
4)4NO2+2H2O+O2->4HNO3
N+4 – 1е→N+5 восстановитель
O20 +4e→2O-2 окислитель
5)Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2NO + 02 2N02 + Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNОз(конц.} →.
ЗАДАНИЕ 4
ЦИНК массой 6,5 кг обработали избытком раствора серной кислоты. Определите объем выделившегося газа, если выход продукта реакции составил 80% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 65000/65 = 1000 моль
n(H2) = n(Zn) = 1000 моль (теор.)
n(H2)практ. = 1000*0,8 = 800моль
V(H2) = 800*22,4 = 17920л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →… →H2S04 →… .
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
S+ Fe = FeS
S0 + 2e = S-2 окислитель
Fe0 -2e= Fe+2 восстановитель
4FeS + 7O2 → 2Fe2O3 + 4SO2↑
S-2 -6e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
2SO2 + O2 = 2SO3
S +4 – 2е→ S +6 восстановитель
O20 +4e→2O-2 окислитель
SO3 + H2O = H2SO4
SO3 + H2O = 2H+ +SO42-
H2SO4 + 2NaOH = Na2SO4 + H2O
2H+ +2OH- = H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО – Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHЦ) →.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии 13 г цинка с избытком раствора серной кислоты? Объемная доля выхода водорода составляет 90% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 13/65 = 0,2 моль
n(H2) = n(Zn) = 0,2 моль (теор.)
n(H2)практ. = 0,2*0,9 = 0,18 моль
V(H2) = 0,18*22,4 = 4,032 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si →…→ Na2Si03 →…→ Si02.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
Si + O2 = SiO2
S0 -4e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
SiO2 + Na2O = 2Na+ +SiO32-
Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2Н+ + SiO32- = H2SiO3 ↓
H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
H20(nap) + C0H2 + C02-Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию в свете ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + … + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
10 кг оксида магния обработали избытком раствора азотной кислоты. Какая масса соли образовалась, если выход соли составил 80% от теоретически возможного?
2HNO3 + MgO = Mg(NO3)2 + H2O
n(MgO) = 1000/40 = 250 моль
n(Mg(NO3)2) = n(MgO) = 250 моль (теор.)
n(Mg(NO3)2)практ. = 250*0,8 = 200 моль
m (Mg(NO3)2) 200*148 = 29600 г