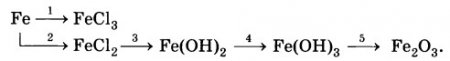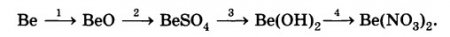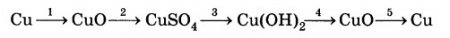Вариант 1
ЗАДАНИЕ 1
Дана схема превращений:
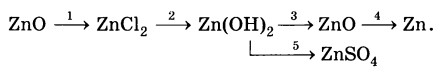
Напишите уравнения химических реакций в молекулярном виде.
Превращение 4 рассмотрите в свете ОВР.
Превращение 5 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 3 по всем изученным признакам классификации.
ZnO + 2HCl = ZnCl2 + H2O
ZnCl2 + 2KOH = Zn(OH)2 + 2KCl
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
2Н+ +2OH- =2H2O
Zn(OH)2 = ZnO + H2O – Q
Реакция разложения. Из 1 ФЕ гидроксида цинка тв.(1 атом цинка, 2 атома водорода, 2 атома кислорода) образуется 1 ФЕ оксида цинка тв.(1 атом цинка ,1 атом кислорода) и 1 молекула вода жидк.(2 атома водорода, 1 атом кислорода). Необратимая. Не овр. Эндотермическая. Некаталитическая
ZnO + C = Zn + CO
Zn+2 +2e = Zn0 окислитель
C0 -2e = C+2 восстановитель
ЗАДАНИЕ 2
Даны вещества, формулы которых:
A. NaOH.
Б. Н3Р04.
В. К2С03.
Г. С2Н2.
Д. ZnO.
Е. С02.
Ж. Са.
З. СН3СООН.
Укажите классы, к которым относятся эти вещества (по составу).
Укажите тип химической связи в веществах А, Е, Ж.
Укажите степень окисления каждого элемента в соединениях Б, В.
Предложите не менее трех способов получения вещества В. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом.
А щелочь, ионная связь
Б кислота Н+13Р+5О-24
В соль К+12С+4О-23
2KOH + CO2 → K2CO3 + H2O
К2О + СО2 = K2CO3
2KНCO3 =K2CO3 + CO2 +H2O
А – с Б, Д, Е, З
Б – с А,В, Д,Ж
Д – с А, Б, Е,З
А также З и Ж
Г алкин
Д оксид
Е оксид, ковалентная полярная связь
Ж металл, металлическая связь
З карбоновая кислота
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при действии раствора азотной кислоты на 75 г карбоната кальция.
2HNO3+CaCO3–>Ca(NO3)2+H2O+CO2
n(CaCO3) = 75/100 = 0,75 моль
n(CO2) = n(CaCO3) = 0,75 моль
V(CO2) = 0,75*22,4 = 16,8 л
ЗАДАНИЕ 1
Дана схема превращений:
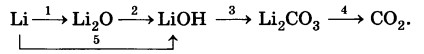
Напишите уравнения химических реакций в молекулярном виде.
Превращение 1 рассмотрите в свете окислительно-восстановительных реакций.
Превращение 4 рассмотрите в свете теории электролитической диссоциации.
Дайте характеристику химической реакции превращения 5 по всем изученным признакам классификации.
4Li+O2=2Li2O
Li0-1e=Li+ восстановитель
O02 +4e=2O-2 окислитель
Li2O+H2O=2LiOH
2LiOH + СО2 = Li2СО3 + Н2О
Li2СО3 + 2HCl = 2LiCl + H2O + CO2
2Н+ +СО32- = H2O + CO2
2Li + 2H2O = 2LiOH + H2 + Q
Li0-1e=Li+ восстановитель
Н2 +2e=2Н-1окислитель
Р. Замещения. Экзотермическая, ОВР, без катализатора, прямая, необратимая.
Исходные: 2 атома лития тв., 2 молекулы воды жидк.(2 атома водорода, 1 атом кислорода). Продукты реакции: 2 ФЕ гидроксида лития раствор(1 атом лития, 1 атом кислорода, 1 атом водорода), 1 молекула водорода газ(2 атома водорода).
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. S02.
Б. КОН.
В. CU(N03)2.
Г. СН3—СН2—ОН.
Д. СuО.
Е. H2S04.
Ж. С2Н4.
3. СН3СООН.
Предложите вариант классификации этих веществ по составу.
Укажите вид химической связи в веществах А, ДиЗ.
Укажите степень окисления каждого элемента в соединениях Д и Е.
Предложите не менее трех способов получения вещества В. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом.
А оксид (неорг.вещество). ковалентная полярная
Б щелочь(неорг.вещество)
В соль (неорг.вещество)
1) CuO+2HNO3=Cu(NO3)2+H2O
2)3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O
3)CuSO4+Pb(NO3)2=Cu(NO3)2+PbSO4↓
Г спирт (орг.вещество)
Д оксид(неорг.вещество) ионная связь Cu+2O-2
Е кислота(неорг.вещество) H+12S+6O-24
Ж алкен(орг.вещество)
З карбоновая кислота(орг.вещество) ковалентная полярная связь
Реагируют:
А – с Б, Д
Б – А,В, Е,З
В – Б
Д – А,З
Е – Б, Д
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем (при н. у.) оксида углерода (IV), полученного при взаимодействии 80 г карбоната кальция с избытком соляной кислоты.
CaCO3 + 2HCl = CaCl2 + CO2 ↑ +H2O
n(CaCO3) = 80/100 = 0,8 моль
n(CO2) = n(CaCO3) = 0,8 моль
V(CO2) = 0,8*22,4 = 17,92 л
ЗАДАНИЕ 1
Дана схема превращений:
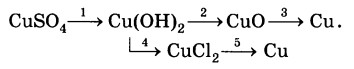
Напишите уравнения химических реакций в молекулярном виде.
Превращение 3 рассмотрите в свете ОВР.
Превращение 1 рассмотрите в свете ТЭД.
Дайте полную характеристику химической реакции превращения 2 по всем изученным признакам классификации.
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4.
Cu2+ + 2OH- = Cu(OH)2↓
Cu(OH)2 → CuO + H2O – Q
Реакция разложения. Из 1 ФЕ гидроксида меди тв.(1 атом меди, 2 атома водорода, 2 атома кислорода) образуется 1 ФЕ оксида меди тв.(1 атом меди ,1 атом кислорода) и 1 молекула вода жидк (2 атома водорода, 1 атом кислорода). Необратимая. Не овр. Эндотермическая. Некаталитическая
CuO + H2 = Cu + H2O
Cu+2+ 2e = Cu0 окислитель
H02 -2e= 2H+восстановитель
Cu(OH)2 + 2HCl = CuCl2 + 2H2O.
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. С2Н6.
Б. НСl.
В. СаО.
Г. Mg.
Д. Zn(OH)2.
Е. Р205.
Ж. MgS04.
3. NaOH.
И. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу).
Укажите вид химической связи в веществах Б, В и Г.
Укажите степень окисления каждого элемента в соединениях Е и 3.
Предложите не менее трех способов получения вещества Ж. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом.
А углеводороды, алканы
Б кислоты, ковалентная полярная
В оксиды, ионная
Г металлы, металлическая
Д гидроксиды
Е оксиды Р+52О-25
Ж соли
MgO + H2SO4 = MgSO4 + H2O
MgO + SO3 = MgSO4
Mg + H2SO4 = MgSO4 + H2↑
З гидроксиды Na+1O-2H+1
И спирты
Взаимодействуют:
Б – с В, Г, Д, З
В – Б, Д, Е
Г – Б, И
Д – Б, В, Е, З, Ж
Е – В, Д, З
Ж – З, Д
З – Б, Д, Е, Ж
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем водорода (н. у.), выделившегося при взаимодействии 13 г цинка с соляной кислотой.
Zn+2HCl=ZnCl2+H2
n(Zn) = 13/65 = 0,2 моль
n(H2) = n(Zn) = 0,2 моль
V(H2) = 0,2*22,4 = 4,48 л
ЗАДАНИЕ 1
Дана схема превращений:
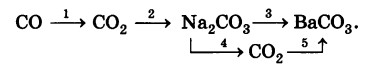
Напишите уравнение химических реакций в молекулярном виде.
Превращение 1 рассмотрите в свете ОВР.
Превращение 3 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 4 по всем изученным признакам классификации.
2СО + О2 = 2СО2
С+2-2e=С+4 восстановитель
O2 +4e=2O-2 окислитель
CO2 + Na2O = Na2CO3
Na2CO3 + BaCl2 = 2NaCl + BaCO3↓
Ba2+ + CO32-=BaCO3↓
Na2CO3 +2HCl = 2NaCl + H2O + CO2↑+ Q
СО32- + 2Н+= H2O + CO2
Р. Обмена. Исходные вещества: 1 моль карбоната натрия (2 атома натрия, 1 атом углерода, 3 атома кислорода) раствор., 2 моль соляной кислоты (в молекуле 1 атом водорода, 1 атом хлора) жидк. Продукты реакции: 2 моль хлорида натрия (в ФЕ 1 атом натрия, 1 атом хлора) раствор., 1 моль воды (2 тома водорода, 1 атом кислорода) жидк., 1 моль углекислого газа (1 атом углерода, 2 атома кислорода) – газ. Реакция:
Экзотермическая.
Без изменения степеней окисления.
Прямая.
Без участия катализатора.
Необратимая.
CO2 + BaO = BaCO3
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. HN03.
Б. CO.
В. Аl203.
Г. С2Н4.
Д. Са(ОН)2.
Е. N2.
Ж. ВаСl2.
3. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу).
Укажите вид химической связи в веществах Б, Е и Ж.
Укажите степень окисления каждого элемента в соединениях А и Е.
Предложите не менее трех способов получения вещества Ж. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом.
А кислота H+1N+5O-23
Б оксид несолеобр., ковалентная полярная
В амфотерный оксид
Г алкен
Д основание (гидроксид)
Е неметалл, ковалентная неполярная N02
Ж соль, ионная
BaO + 2HCl–>BaCl2 + H2O
Ba(OH)2 + 2 HCl –> BaCl2 + 2 H2O
BaCO3 + 2 HCl —> BaCl2 + H2O + CO2
З спирт
Реагируют
А – с В, Д
В – А, Д
Д – А, В
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при взаимодействии 40 г карбоната кальция с избытком соляной кислоты.
CaCO3 + 2HCl = CaCl2 + CO2 ↑ +H2O
n(CaCO3) = 40/100 = 0,4 моль
n(CO2) = n(CaCO3) = 0,4 моль
V(CO2) = 0,4*22,4 = 8,96 л
Вариант 1
ЗАДАНИЕ 1
Дана схема превращений:
Напишите уравнения химических реакций в молекулярном виде.
Превращение 4 рассмотрите в свете ОВР.
Превращение 3 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 1 по всем изученным признакам классификации.
2Fe + 3Cl2 = 2FeCl3 + Q,
2 Fe – 3e– = Fe+III, 2Fe – 6e– = 2Fe+III,
3 Cl2 + 2e– = 2Cl–I, 3Cl2 + 6e– = 6Cl–I.
Fe – 3e– = Fe+III восстановитель
Cl2 + 2e– = 2Cl–I окислитель
Р. Замещения. Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль железа – тв., 2 моль хлора (молекула из 2 атомов) – газ
Продукт: 2 моль хлорида железа (из 1 атома железа, 2 атомов хлора в ФЕ) – тв.
Fe + 2HCl = FeCl2 + H2
FeCl2 + 2NaOH –> Fe(OH)2 + 2NaCl
Fe2+ + 2OH- –> Fe (OH)2
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
Fe2+ -1е→ Fe3+ восстановитель
O20 + 4е→ 2O2- окислитель
2Fe(OH)3 = Fe2O3 + 3H2O (при нагревании)
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. NaOH.
Б. Н3Р04.
В. К2С03.
Г. С2Н2.
Д. ZnO.
Е. С02.
Ж. Са.
3. СН3СООН.
Укажите классы, к которым относятся эти вещества (по составу и свойствам).
Укажите вид химической связи в веществах А, ЖиЗ.
Укажите степень окисления каждого элемента во всех соединениях.
Предложите не менее четырех способов получения вещества В. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом с образованием солей. Напишите два уравнения реакции в ионном виде.
А щелочь, гидроксид. Ионная связь. Na+1O-2H+1
Б неорганическая кислота. H+13P+5O-24
В средняя соль. K+12C+4O-23
2KOH + CO2 → K2CO3 + H2O
К2О + СО2 = K2CO3
2KНCO3 =K2CO3 + CO2 +H2O
К2О + H2CO3 = K2CO3 + H2O
Г углеводород, алкин/ C-12H+12
Д амфотерный оксид. Zn+2O-2
Е кислотный окисд. C+4O-22
Ж простое вещество металл. Металлическая связь. Ca0
З органическая карбоновая кислота. Ковалентная полярная связь. C-3H+13C+3O-2O-2H+1
Реагируют:
А – Б, Д, Е, З
Б – А, В, Д, Ж
В – Б, З
Д – Е ,З А, Б
H3PO4 + 3NaOH=Na3PO4+3H2O
3H+ + 3OH-= 3H2O
ZnO+CO2 = ZnCO3
ZnO+CO2 = Zn2+ +CO32-
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при действии раствора, содержащего 126 кг азотной кислоты с избытком карбоната кальция.
2HNO3+CaCO3 →Ca(NO3)2+H2O+CO2
n(HNO3) = 126000/63 = 2000 моль
n(CO2) = n(HNO3) /2= 1000моль
V(CO2) = 1000*22,4 = 22400 л
ЗАДАНИЕ 1
Дана схема превращений:
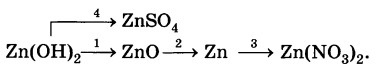
Напишите уравнения химических реакций в молекулярном виде.
Превращение 2 рассмотрите в свете ОВР.
Превращение 4 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 1 по всем изученным признакам классификации.
Zn(OH)2= ZnO + H2O- Q
Реакция разложения. Из 1 ФЕ гидроксида цинка тв.(1 атом цинка, 2 атома водорода, 2 атома кислорода) образуется 1 ФЕ оксида цинка тв.(1 атом цинка ,1 атом кислорода) и 1 молекула вода жидк.(2 атома водорода, 1 атом кислорода). Необратимая. Не овр. Эндотермическая. Некаталитическая
ZnO + C = Zn + CO
Zn+2 +2e = Zn0 окислитель
C0 – 2e = C+2 восстановитель
Zn + 4HNO3(конц.) = 2NO2↑ + 2H2O + Zn(NO3)2
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
2Н+ + 2OH- =2H2O
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. S02.
Б. КОН.
В. CU(N03)2.
Г. СН3—СН2—ОН.
Д. СuО.
Е. H2S04.
Ж. С2Н4.
3. СН3СООН.
Предложите вариант классификации этих веществ по составу и по свойствам.
Укажите вид химической связи в веществах А, Б и Д.
Укажите степень окисления каждого элемента в соединениях А, Б, В, Д и Е .
Предложите не менее четырех способов получения вещества В. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом с образованием солей. Напишите два уравнения реакции в ионном виде.
А кислотный оксид S+4O-22. Ковалентная полярная связь
Б основание, щелочь К+1О-2Н+1 Ионная связь
В средняя соль Cu+2(N+5O-23)2
3Cu + 8HNO3 (разб.) = NO ↑ + 3Cu(NO3)2+ 4H2O
Cu + 4HNO3 (конц.) = 2NO2↑ + 2H2O + Cu(NO3)2
Сu(OH)2+2HNO3=>Cu(NO3)2+2H2O
CuO+2HNO3=Cu(NO3)2+H2O
Г спирт этанол C-3H+13 – C-1H+12 – O-2H+1
Д основной оксид Cu+2O-2 Ионная связь
Е неорганическая кислотаH+12S+6O-24
Ж углеводород алкен С-22Н+14
З органическая карбоновая кислота. Ковалентная полярная связь. C-3H+13C+3O-2O-2H+1
Реагируют:
А и Б, Д
Б – А, В, Е, З
Д – З
H2SO4+2KOH=K2SO4+2H2O
2Н+ + 2OH- =2H2O
2KOH + SO2 = K2SO3 +H2O
2OH- + SO2 = SO32- +H2O
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем (при н. у.) оксида углерода (IV), полученного при взаимодействии 80 г карбоната кальция с избытком соляной кислоты.
2HNO3+CaCO3 →Ca(NO3)2+H2O+CO2
n(CaCO3) = 80/100 = 0,8 моль
n(CO2) = n(CaCO3) = 0,8 моль
V(CO2) = 0,8*22,4 = 17,92 л
m(CO2) = 0,8*44 = 35,2 г
ЗАДАНИЕ 1
Дана схема превращений:
Напишите уравнения химических реакций в молекулярном виде.
Превращение 1 рассмотрите в свете ОВР.
Превращение 4 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 2 по всем изученным признакам классификации.
2 Ве + O2 = 2 ВеО
Ве0 -2e→ Ве 2+ окисляется, восстановитель
О20+4e→2 О 2- восстанавливается, окислитель
BeO + H2SO4 → BeSO4 + H2O + Q
Р. Обмена. Экзотермическая, не ОВР, без катализатора, прямая, необратимая.
Исходные: 1 ФЕ оксида бериллия тв., 1 молекула серной кислоты жидк.(2 атома водорода, 4 атома кислорода, 1 атом серы). Продукты реакции: 1 ФЕ сульфата бериллия раствор.(1 атом бериллия, 4 атома кислорода, 1 атом серы), 1 молекула воды жидк.(2 атома водорода, 1 атом кислорода).
2KOH + BeSO4 → K2SO4 + Be(OH)2↓
Be (OH)2 + 2HNO3 = Be (NO3)2 + 2H2O
2OH- + 2H+ = 2H2O
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. С2Н6.
Б. НСl.
В. СаО.
Г. Mg.
Д. Zn(OH)2.
Е. Р205.
Ж. MgS04.
3. NaOH.
И. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу и свойствам).
Укажите вид химической связи в веществах В, 3 и И.
Укажите степень окисления каждого элемента во всех соединениях.
Предложите не менее четырех способов получения вещества Ж. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом с образованием солей. Напишите два уравнения реакции в ионном виде.
А С-32Н+16 алкан, углеводород
Б H+1Cl-1 неорг.кислота
В Са+2О-2 оксид основный, ионная связь
Г Mg0 – металл, простое вещество
Д Zn+2(O-2H+1)2 – гидроксид амфотерный
Е Р+52О-25 – кислотный оксид
Ж Mg+2S+6O-24 – средняя соль
MgO + H2SO4 = MgSO4 + H2O
MgO + SO3 = MgSO4
Mg + H2SO4 = MgSO4 + H2↑
Mg(OН)2 + H2SO4 = MgSO4 + 2H2O
З Na+1O-2H+1 – гидроксид, щелочь, ионная связь
И С-2Н+13О-2Н+1 – одноатомный спирт, ковалентная связь
Б – В, Г, Д, З
В – Б, Д, Е
Г – Б
Д – Б, В, Е, Ж, З
Ж – З
Е – З
NaOH+HCl=NaCl+H2O
Н+ + ОН- = Н2О
СаО + 2HCl = СаCl2 + Н2О
СаО + 2H+ = Са2+ + Н2О
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем водорода (н. у.), выделившегося при взаимодействии 13 г цинка с избытком соляной кислоты.
Zn+2HCl=ZnCl2+H2
n(Zn) = 13/65 = 0,2 моль
n(H2) = n(Zn) = 0,2 моль
V(H2) = 0,2*22,4 = 4,48 л
m(Н2) = 0,2*2 = 0,4 г
ЗАДАНИЕ 1
Дана схема превращений:
Напишите уравнения химических реакций в молекулярном виде.
Превращение 4 рассмотрите в свете ОВР.
Превращение 2 рассмотрите в свете ТЭД.
Дайте характеристику химической реакции превращения 3 по всем изученным признакам классификации.
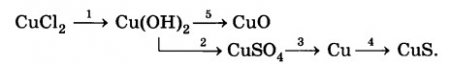
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
Cu(OH)2 + H2SO4 = Cu SO4 + 2H2O
Cu(OH)2 + 2H+ + SO42- = Cu2+ + SO42- + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2О.
Fe +CuSO4= FeSO4 +Cu + Q
Fe0 – 2e– = Fe+II восстановитель
Cu+2 + 2e– = Cu 0 окислитель
Р. Замещения. Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 1 моль железа – тв., 1 сульфата меди (ФЕ из 1 атома меди, 1 атом серы, 4 атома кислорода) – раствор.
Продукты: 1 моль меди, 1 моль сульфата железа-2 (ФЕ из 1 атома железа, 1 атом серы, 4 атома кислорода) – раствор.
Cu + S = CuS
Cu0 -2е = Cu+2 восстановитель
S0 +2е= S-2 окислитель
Cu(OH)2 = CuO + H2O
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. HN03.
Б. CO.
В. Аl203.
Г. С2Н4.
Д. Са(ОН)2.
Е. N2.
Ж. ВаСl2.
3. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу и по свойствам).
Укажите вид химической связи в веществах Б, Е и Ж.
Укажите степень окисления каждого элемента во всех соединениях.
Предложите не менее четырех способов получения вещества Ж. Запишите соответствующие уравнения реакций.
Укажите вещества, которые попарно взаимодействуют друг с другом с образованием солей. Напишите два уравнения реакции в кратком ионном виде.
А H+1N+5O-23 кислота
Б C+2O-2 несолеобразующий оксид, ковалентная полярная
В Al+32O-23 амфотерный окисд
Г C-22H+14 углеводород , алкен,
Д Ca+2 (O-2H+1)2 гидроксид, основание
Е N02 простое вещество, неметалл, ковалентная неполярная
Ж Ba+2Cl-12 соль, ионная
BaO + 2HCl–>BaCl2 + H2O
Ba(OH)2 + 2 HCl –> BaCl2 + 2 H2O
BaCO3 + 2 HCl —> BaCl2 + H2O + CO2
Ba + Cl2–>BaCl2
З С-2Н+13О-2Н+1 спирт
А – с В, Д
В – А, Д
Д – Ж
Ca(OH)2+ 2HNO3= Ca(NO3)2 +2H2O
2Н+ + 2ОН- = 2Н2О
Al2O3 + 6HNO3 = 2Al(NO3)3 + 3H2O
Al2O3 + 6H+ = 2Al3+ + 3H2O
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при взаимодействии 40 г карбоната кальция с избытком соляной кислоты.
CaCO3 + 2HCl = CaCl2 + CO2 ↑ +H2O
n(CaCO3) = 40/100 = 0,4 моль
n(CO2) = n(CaCO3) = 0,4 моль
V(CO2) = 0,4*22,4 = 8,96 л
m(CO2) = 0,4*44 = 17,6 г
Вариант 1
ЗАДАНИЕ 1
Дана схема превращений:
Напишите уравнения химических реакций в молекулярном виде.
Два превращения рассмотрите в свете ОВР.
Два превращения рассмотрите в свете ТЭД.
Дайте характеристику реакции замещения по всем изученным признакам классификации.
2Cu + O2 = 2CuO
Cu0 -2е = Cu2+восстановитель
O02 +4е= 2O-2 окислитель
CuO + H2SO4 = Cu SO4 + H2O
CuO + 2H+= Cu2++ H2O
Ca(OH)2 + Cu SO4 → Cu(OH)2↓ + CaCl2
Cu2+ + 2 OH- → Cu(OH)2↓
Cu(OH)2 = CuO + H2O
CuO + H2 = Cu + H2O + Q
Cu2+ -2е = Cu0 окислитель
Н02 +2е= 2Н+ восстановитель
Исходные вещества: Р. Замещения. 1 моль окисда меди тв. (в ФЕ 1 атом меди, 1 атом кислорода), 1 моль водорода газ (2 атома водорода в молекуле). Продукты реакции: 1 моль меди тв.(1 атом меди), 1 моль воды жидк.(2 атома водорода, 1 атом кислорода в молекуле).
Экзотермическая реакция
Без катализатора
С изменением степеней окисления. Прямая, необратимая.
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. NaOH.
Б. Н3Р04.
В. К2С03.
Г. С2Н2.
Д. ZnO.
Е. С02.
Ж. Са.
3. СН3СООН.
Дайте полную классификацию этих веществ, назовите вещества.
Укажите вид химической связи во всех веществах.
Укажите степень окисления каждого элемента во всех соединениях.
Напишите по одному уравнению химической реакции, подтверждающему химические свойства веществ Ж и 3.
Укажите вещества, которые попарно взаимодействуют друг с другом.
Напишите уравнение реакции нейтрализации, выбрав вещества из перечисленных выше.
А Na+1O-2H+1 гидроксид натрия, сл.вещество, основание, щелочь. Ионная связь
Б H+13P+5O-24 фосфорная кислота, сл.ве-во, кислота неорганическая. Ковалентная полярная
В K+12C+4O-23 карбонат калия, средняя соль, сл.ве-во. Ионная
Г C-12H+12 ацетилен, углеводород, алкин, сл. Вещество органич. Ковалентная полярная
Д Zn+2O-2 оксид цинка, сл. Вещество, неорганич., амфотерный оксид. Ионная
Е C+4O-22 окисд углерода 4, сл. Неорганическое вещество, кислотный оксид. Ковалентная полярная
Ж Ca0 простое вещество металл, кальций. Металлическая.
Ca+2HCl = CaCl2+H2
З C-3H+13C+3O-2O-2H+1 уксусная (этановая) кислота, сл. Органическое вещество, одноосновные насыщенные карбоновые кислоты. Ковалентная полярная.
Реагируют:
А – Б, Д, Е, З
Б – В, Д, Ж
В – З
Д – Е, З
Е – Г
Ж – З
H3PO4 + 3NaOH = Na3PO4 + 3H2O
CH3COOH+NaOH =>CH3COONa+H2O
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при действии раствора, содержащего 126 кг азотной кислоты, на избыток карбоната кальция, если выход углекислого газа составляет 80% от теоретически возможного.
2HNO3+CaCO3 →Ca(NO3)2+H2O+CO2
n(HNO3) = 126000/63 = 2000 моль
n(CO2) = n(HNO3) /2= 1000моль(теор.)
n(CO2)практ. = 1000*0,8 = 800 моль
V(CO2) = 800*22,4 = 17920 л
m(CO2) =800*44 = 35200 г
ЗАДАНИЕ 1
Дана схема превращений:
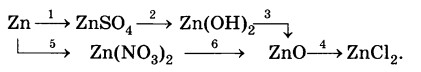
Напишите уравнения химических реакций в молекулярном виде.
Два превращения рассмотрите в свете ОВР.
Два превращения рассмотрите в свете ТЭД.
Дайте характеристику реакции замещения по всем изученным признакам классификации.
Zn+CuSO4 →ZnSO4 +Cu + Q
Zn 0 + Cu2+ = Zn 2+ + Cu0
Zn 0 – 2e = Zn 2+ восстановитель
Cu2+ + 2e= Cu0 окислитель
Исходные вещества: 1 моль цинк тверд, 1 моль сульфата меди раствор(1 атом меди, 1 атом серы, 4 атома кислорода в ФЕ). Продукты реакции: 1 моль меди, 1 моль сульфата цинка раствор(1 атом цинка, 1 атом серы, 4 атома кислорода в ФЕ.
Р.замещения. Экзотермическая реакция
Без катализатора
С изменением степеней окисления
Необратимая
ZnSO4+2NaOH=Zn(OH)2↓+H2O
Zn2++2OH-=Zn(OH)2↓
Zn(OH)2= ZnO + H2O
Zn + 4HNO3 = Zn(NO3)2 + 2NO2 + 2H2O
Zn0 -2е =Zn+2 восстановитель
N+5 + 1е=N+4 окислитель
2Zn(NO3)2= 2ZnO+4NO2+O2
2HCl+ZnO=ZnCl2+H2O
2H++ZnO=Zn2++H2O
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. S02.
Б. КОН.
В. Cu(N03)2.
Г. СН3—СН2—ОН.
Д. СuО.
Е. H2S04.
Ж. С2Н4.
3. СН3СООН.
Дайте полную классификацию этих веществ, назовите вещества.
Укажите вид химической связи во всех веществах.
Укажите степень окисления каждого элемента в соединениях А, Б, В, Г, Д.
Напишите по одному уравнению химической реакции, подтверждающему химические свойства веществ Г и Ж.
Укажите вещества, которые попарно взаимодействуют друг с другом. Напишите уравнения реакций нейтрализации в ионном виде.
А S+4O-22 оксид серы 4, кислотный. Ковалентная полярная
Б K+1O-2H+1 – щелочь, гидроксид калия. Ионная
В Cu+2O-2 оксид меди 2, основной. Ионная
Г H+12S+6O-24 серная кислота. Ковалентная полярная
Zn + H2SO4 = ZnSO4 + H2
Д Cu+2 (N+5O-23)2 нитрат меди 2. Соль. Ионная
Е C-3H3 – C-1H2 – OH одноатомный насыщенный спирт, этанол. Ковалентная полярная
Ж C2H+14 углеводород, алкен. Ковалентная полярная
CH2 = CH2 + Br2 → Br – CH2 – CH2 -Br
З C-3H+13C+3O-2O-2H+1. Насыщенная карбоновая кислота, уксусная (этановая). Ковалентная полярная
Реагируют:
А – В, Б
Б – Г,З
В – Г,З
Е – З
H2SO4+2KOH=K2SO4+2H2O
2H++2OH-=2H2O
CH3COOH + KOH = CH3COOK + H2O
H++OH-=H2O
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем (при н. у.) оксида углерода (IV), полученного при взаимодействии 80 г карбоната кальция с избытком соляной кислоты. Выход углекислого газа составляет 80% от теоретически возможного.
CaCO3 + 2HCl = CaCl2 + CO2 ↑ +H2O
n(CaCO3) = 80/100 = 0,8 моль
n(CO2) = n(CaCO3) = 0,8 моль (теор.)
n(CO2) (практ.)= 0,8*0,8=0,64 моль
V(CO2) = 0,64*22,4 = 14,336 л
m(CO2) = 0,64*44 = 28,16 г
ЗАДАНИЕ 1
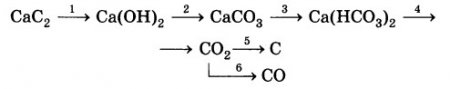
Дана схема превращений:
Напишите уравнения химических реакций в молекулярном виде.
Два превращения рассмотрите в свете окислительно-восстановительных реакций.
Два превращения рассмотрите в свете теории электролитической диссоциации.
Дайте характеристику реакции разложения по всем изученным признакам классификации.
CaC2 + 2H2O ⇒ C2H2 + Ca(OH)2
Ca(OH)2+CO2=CaCO3+H2O
Ca2+ +2OH-+CO2=CaCO3+H2O
CaCO3+CO2+H2O=Ca(HCO3)2
Ca(HCO3)2→темп.→CaCO3↓+CO2↑+H2O – Q
Реакция разложения. Из 1 ФЕ гидрокарбоната кальция раствор.(1 атом кальция, 2 атома водорода, 6 атома кислорода, 2 атома углерода) образуется 1 ФЕ карбоната кальция тв.(1 атом кальция ,1 атом углерода, 3 атома кислорода), 1 молекула углекислого газа (1 атом углерода, 2 атома кислорода) и 1 молекула вода жидк (2 атома водорода, 1 атом кислорода). Необратимая. Не овр. Эндотермическая. Некаталитическая
Ca2+ +2HCO3-→CaCO3+CO2+H2O
2Mg + CO2 = 2MgO + C
Mg0 -2е = Mg+2 восстановитель
C+4 +4е= C0 окислитель
С + СО2 = 2СО
С0 -2е = С+2 восстановитель
С+4 + 2е = С+2 окислитель
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. С2Н6.
Б. НСl.
В. СаО.
Г. Mg.
Д. Zn(OH)2.
Е. Р205.
Ж. MgS04.
3. NaOH.
И. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу и свойствам).
Укажите вид химической связи во всех веществах.
Укажите степень окисления каждого элемента во всех соединениях.
Напишите по одному уравнению химической реакции, подтверждающему химические свойства веществ Е и И.
Укажите вещества, которые попарно взаимодействуют друг с другом. Напишите уравнение реакции нейтрализации в ионном виде.
А С-32Н+16 алканы, углеводорода, этан. Ковалентная полярная
Б H+1Cl-1неорганические кислоты, хлороводородная. Ковалентная полярная
В Ca+2O-2 основные оксиды, оксид кальция. Ионная
Г Mg0. Металлы, простые вещества. Металлическая
Д Zn+2(O-2H+1)2. Гидроксиды, амфотерные. Гидроксид цинка. Ионная
Е P+52О-25. Оксиды кислотные. Оксид фосфора 5. Ковалентная полярная
P2O5 + 3H2O = 2H3PO4
Ж Mg+2S+6O-24. Средние соли. Сульфат магния. Ионная
З Na+1O-2H+1. Гидроксиды, щелочи. Гидроксид натрия. Ионная
И С-2Н+13О-2Н+1. Одноатомные насыщенные спирты. Метиловый спирт. Ковалентная полярная.
СНзОН + СНзСООН —> СНзСООСНз + Н2О
Реагируют:
Б – В,Г,Д,З, И
В – Д,Е
Г – И
Д – Е, З
Е – З
Ж – З
NaOH + HCl –>NaCl + H2O
Н+ +ОН- = Н2О
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте объем водорода (н. у.), выделившегося при взаимодействии 13 г цинка с избытком соляной кислоты. Выход водорода составил 80% от теоретически возможного.
Zn+2HCl=ZnCl2+H2
n(Zn) = 13/65 = 0,2 моль (теор)
n(Zn) практ.= 0,2 моль *0,8 = 0,16 моль
n(H2) = n(Zn) = 0,16 моль
V(H2) = 0,16*22,4 = 3,584 л
ЗАДАНИЕ 1
Дана схема превращений:
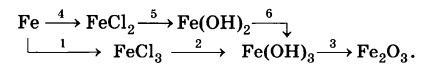
Напишите уравнение химических реакций в молекулярном виде.
Два превращения рассмотрите в свете ОВР.
Два превращения рассмотрите в свете ТЭД.
Дайте характеристику реакции соединения по всем изученным признакам классификации.
2Fe + 3Cl2 = 2FeCl3 + Q
2 Fe – 3e– = Fe+III, 2Fe – 6e– = 2Fe+III,
3 Cl2 + 2e– = 2Cl–I, 3Cl2 + 6e– = 6Cl–I.
Fe – 3e– = Fe+III восстановитель
Cl2 + 2e– = 2Cl–I окислитель
Р. Замещения. Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль железа – тв., 2 моль хлора (молекула из 2 атомов) – газ
Продукт: 2 моль хлорида железа (из 1 атома железа, 2 атомов хлора в ФЕ) – тв.
FeCl3+ 3NaOH → Fe(OH)3 ↓ + 3NaCl
Fe3+ + 3OH- → Fe (OH)3
2Fe(OH)3 t → Fe2O3 + H2O
Fe + 2HCl = FeCl2 + H2
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
Fe2+ + 2OH- → Fe (OH)2
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
Fe2+ -1е→ Fe3+ восстановитель
O20 + 4е→ 2O2- окислитель
ЗАДАНИЕ 2
Даны вещества, формулы которых:
А. HN03.
Б. CO.
В. Аl203.
Г. С2Н4.
Д. Са(ОН)2.
Е. N2.
Ж. ВаСl2.
3. СН3ОН.
Укажите классы, к которым относятся эти вещества (по составу и свойствам).
Укажите вид химической связи во всех веществах.
Укажите степень окисления каждого элемента во всех соединениях.
Напишите по одному уравнению химической реакции, подтверждающему химические свойства веществ Г и 3.
Укажите вещества, которые попарно взаимодействуют друг с другом. Напишите уравнения реакций нейтрализации в ионном виде.
А H+1N+5O-23 неорганическая азотная кислота, ковалентная полярная
Б C+2O-2 несолеобразующий оксид, окисд углерода 2, ковалентная полярная
В Al+32O-23 амфотерный оксид алюминия, ионная
Г C-22H+14 углеводород , алкен, этилен, ковалентная полярная
CH2 = CH2 + Br2 → Br – CH2 – CH2 -Br
Д Ca+2 (O-2H+1)2 гидроксид кальция, основание, ионная
Е N02 простое вещество, неметалл, азот, ковалентная неполярная
Ж Ba+2Cl-12 средняя соль, хлорид бария, ионная
З С-2Н+13О-2Н+1 одноатомный насыщенный спирт метанол., ковалентная полярная
СНзОН + СНзСООН→ СНзСООСНз + Н2О
А – с В, Д
В – А, Д
Д – Ж
Ca(OH)2+ 2HNO3= Ca(NO3)2 +2H2O
2Н+ + 2ОН- = 2Н2О
ЗАДАНИЕ 3 (дополнительное)
Рассчитайте массу и объем углекислого газа (н. у.), выделившегося при взаимодействии 40 г карбоната кальция с избытком соляной кислоты. Выход углекислого газа составил 75% от теоретически возможного.
CaCO3 + 2HCl = CaCl2 + CO2 ↑ +H2O
n(CaCO3) = 40/100 = 0,4 моль (теор.)
n(CO2) (теор.)= n(CaCO3) = 0,4 моль
n(CO2) (практ.) = 0,4*0,75 =0,3 моль
V(CO2) = 0,3*22,4 = 6,72 л
m(CO2) = 0,3*44 = 13,2 г